

近日,上海交通大学变革性分子前沿科学中心刘家旺团队在构型超稳定轴手性苯乙烯合成上取得重要进展,报道了钯催化1,5-烯炔的不对称环化/羰基化反应,成功制备出一系列构型超稳定的轴手性苯乙烯,为新型手性配体的发展提供了新的稳定骨架。相关成果以“Atroposelective Synthesis of Ultrarigid Chiral Styrenes via Pd-Catalyzed Unconventional 5-exo-dig Cyclization/Carbonylation of 1,5-Enynes”为题发表在《Angew. Chem. Int. Ed.》上。

新型手性骨架的设计与合成极大地推动了手性化学领域的发展,吸引了合成化学家们的广泛关注。在过去几十年里,轴手性联芳烃的研究已经取得显著进展,并在天然产物合成、药物化学、不对称催化以及材料科学中得到广泛应用。近年来,新型手性阻转异构体的合成与应用受到广泛关注,尤其是乙烯基-芳基阻转异构体,其结构与轴手性联芳基具有较高的相似性。虽然这类手性结构早在上世纪90年代就已经被合成出来并命名,但其催化不对称合成则发展缓慢,主要难点有:(1)柔性的构象导致其阻转能垒较低,产物易消旋;(2)同时控制反应的多重选择性,包括烯烃顺反、区域和对映选择性。在众多乙烯基-芳基阻转异构体中,含有环外双键的四取代轴手性烯烃是一类构象稳定的结构,研究表明通过烯烃和环状结构的刚性设计,能有效提升产物的阻转能垒,但由于双键周围的基团之间相互排斥导致结构扭曲,其不对称合成更具挑战性。
金属氢催化的非共轭1,n-烯炔不对称环化反应近来已成为高效构建手性环状化合物的有效策略。经典的反应机理认为,原位生成的金属氢物种优先插入活性更高的炔烃,随后与烯烃发生分子内5/6/7-endo/exo-trig环化(图1b右,路径a)。值得注意的是,迄今为止所有报道均聚焦在构建中心手性化合物,利用此策略合成轴手性结构尚属空白。为此,作者设想了一条反应顺序反转的环化路径,即金属氢物种优先加成到烯烃,再与炔烃发生分子内环化的过程(图1b左,路径b)。然而,这种非常规的5-exo-dig环化必须逆转烯炔体系中金属氢物种的反应顺序。因此,设计烯烃优先发生反应的烯炔底物,并开发高效的催化氢官能化反应体系,是获取这类轴手性分子的关键。
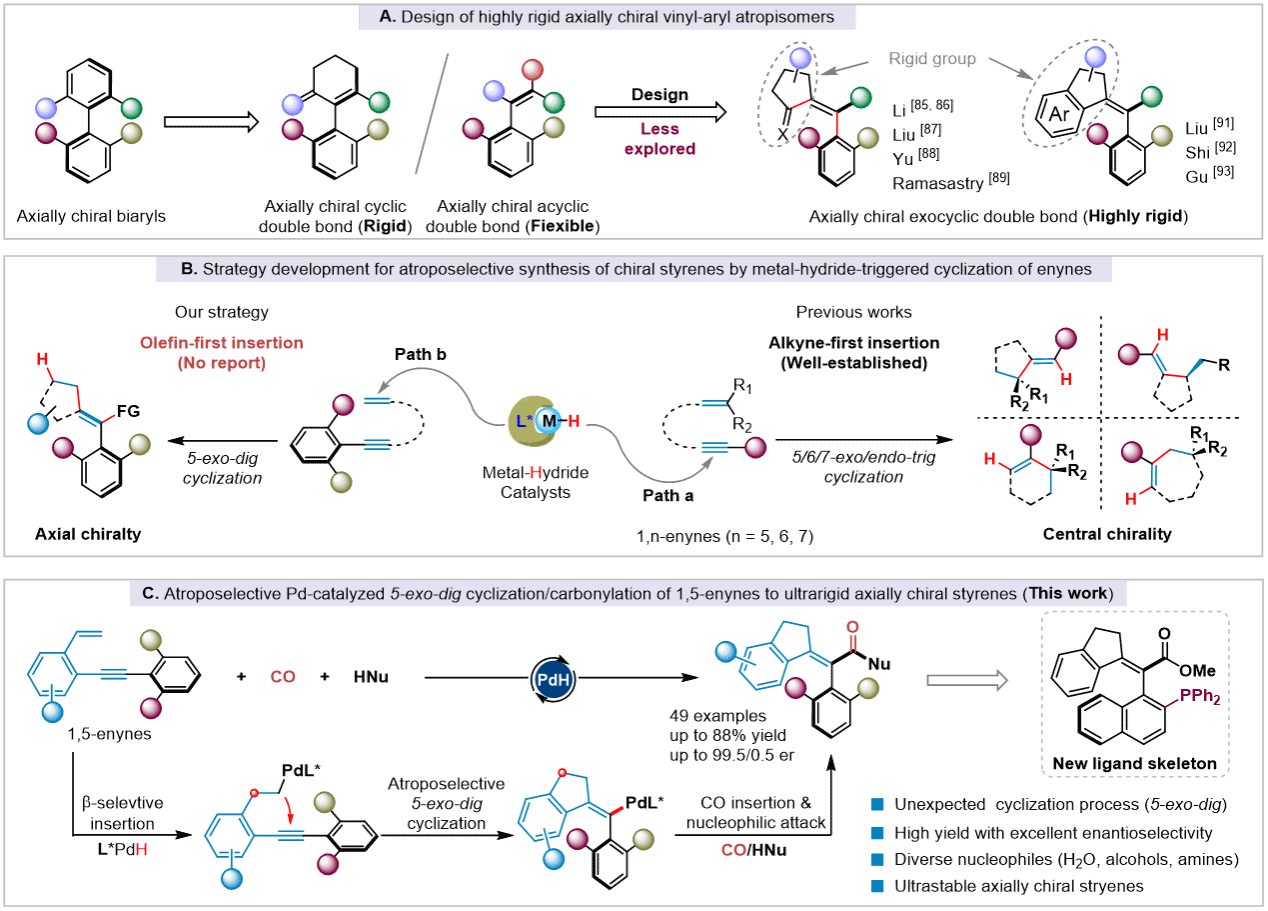
图1. 研究背景以及本工作的反应设计
为了实现上述目标,刘家旺团队基于前期在轴手性化合物合成以及羰基化反应开发方面的经验(J. Am. Chem. Soc. 2025, 147, 23946;Angew. Chem. Int. Ed. 2025, 64, e202413949;Nat. Commun. 2024, 15, 7248;Angew. Chem. Int. Ed. 2025, 64, e202413949),基于以下几点考虑,设计了邻位炔烃取代的苯乙烯底物:(1)烯烃和炔烃之间芳基的引入,不仅能够提供产物环外双键的刚性基团,增强产物稳定性,还能将烯烃部分变为端位苯乙烯,烯烃反应活性得到提升;(2)芳基的引入以及炔烃末端芳基邻位大位阻官能团的引入,增大了炔烃的空间位阻,使炔烃的反应活性降低。通过底物的理性设计,有效调整了烯炔底物中烯烃和炔烃的反应活性,成功实现了钯催化1,5-烯炔的不对称环化/羰基化反应,高效合成了一系列构型超稳定的轴手性苯乙烯,为轴手性苯乙烯的不对称合成与应用提供了新策略。
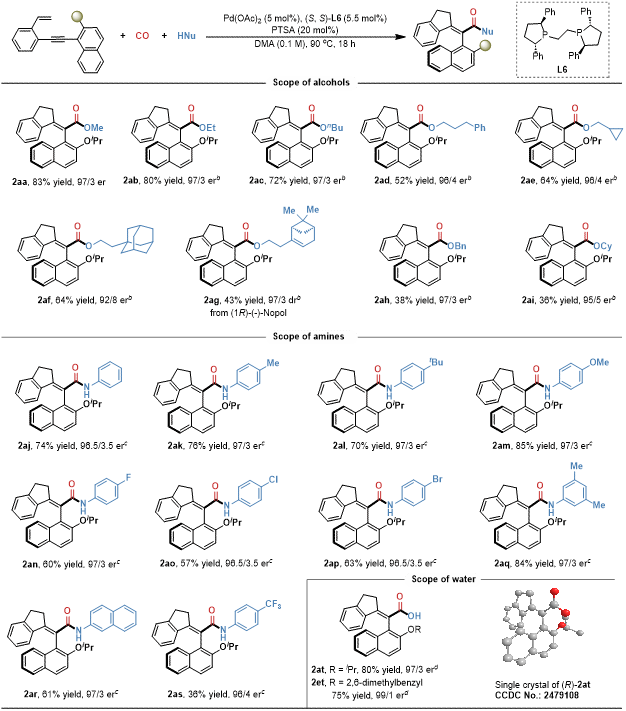
图2. 亲核试剂底物范围考察
作者以2-异丙氧基-1-((2-乙烯基苯基)乙炔基)萘1a作为模板底物,甲醇作为亲核试剂,以Pd(OAc)2作为催化剂,(S, S)-Ph-BPE (L6)为手性配体,对甲苯磺酸作为酸,N,N-二甲基乙酰胺作为反应溶剂,在10 大气压的 CO氛围下90 ℃反应18小时即能以83%的分离产率以及97:3 er值分离得到轴手性甲酯产物2aa。在最优条件下,作者考察了不同种类亲核试剂在反应中的兼容性(图2)。结果表明,多种醇、胺以及水作为亲核试剂,都能以较好的产率和对映选择性得到所需要的轴手性苯乙烯羰基化合物。随后,作者系统考察了烯炔底物取代基对反应活性及对映选择性的影响(图3)。研究表明,烯炔底物萘环邻位上的取代基位阻对反应的对映选择性有较大影响,产物的er值随着取代基位阻增大而增加。其他位置的取代基对反应的影响不大,都能以中等至良好的收率和优秀的对映选择性得到目标产物。

图3. 1,5-烯炔底物范围考察
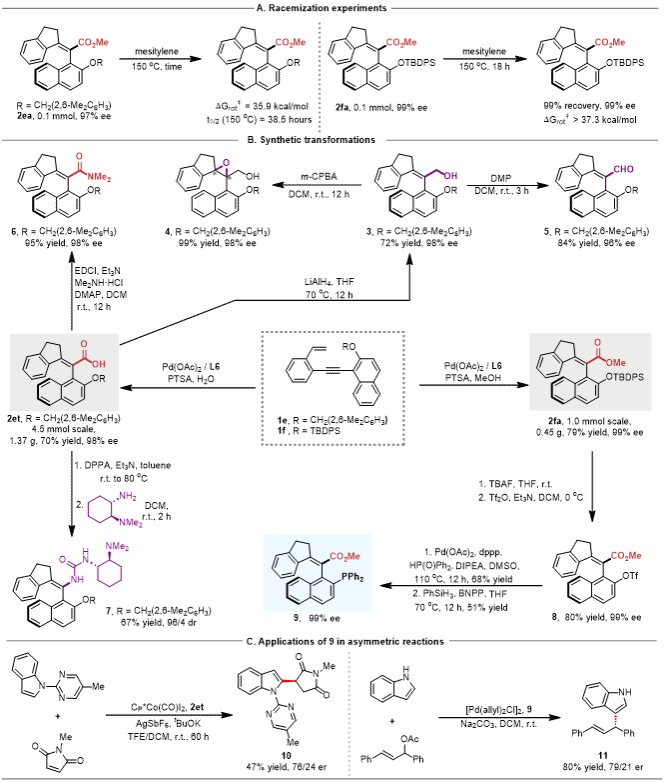
图4 合成应用
在得到这些轴向手性苯乙烯后,作者以2ea和2fa为代表,测定了它们的旋转能垒(ΔGrot‡),以评估构型稳定性(图4a)。结果表明,2ea的ΔGrot‡ 为 35.9 kcal mol⁻¹,对应150 °C下半衰期38.5 h(图4a,左);而2fa的ΔGrot‡ 更高,在同等温度下18 h内未观察到任何消旋现象。这些结果证明了作者设计的轴手性环外四取代烯烃的超稳定结构(图4a,右)。作者进一步对这两种保护基产物进行了放大和后续官能团转化(图4b),包括还原、氧化和Curtius重排等反应。值得一提的是,作者基于合成的构象稳定骨架,发展了一类全新的轴手性苯乙烯单膦配体,并在钯催化不对称烯丙基取代反应中初步证明了其手性诱导能力。
为探究反应机理,作者进行了一系列控制实验:在标准条件下以甲醇作为亲核试剂,对一系列不同底物进行了对照实验(图5A)。首先,含有内烯结构单元的1,5-烯炔13或含有烷基烯烃的1,6-烯炔14在标准条件下均不反应,表明底物中的末端苯乙烯结构单元不可或缺。有趣的是,当使用没有邻位炔基取代的简单苯乙烯(15和16)时,均未观察到烷氧羰基化产物,说明炔基部分对启动羰基化过程至关重要。此外,虽然二苯乙炔可顺利发生烷氧羰基化,并以77%产率得到17,但空间位阻更大的二芳基炔仅以极低产率给出化合物18,说明大位阻的炔烃底物在催化体系下活性确实有所降低。以上结果证明,作者最初设计的1,5-烯炔化合物中苯乙烯结构单元对启动该羰基化反应起关键作用,并且空间位阻大的炔基部分对改变Pd-H物种的插入顺序也十分重要。为进一步验证该Pd/(S, S)-L6催化羰基化优先启动在烯烃单元而非炔烃单元上,用MeOD对1-(苯乙炔基)-3-乙烯基苯19进行氘标记实验(图5C,左),以44%的产率观察到炔烃羰基化产物20,区域选择性为1/1。有趣的是,未反应的乙烯基上检测到34-43%的氘标记,表明Pd-H物种可以插入烯烃,但随后的羰基化反应并未发生,而是可逆的发生β-氢消除。这些结果表明,手性配体的选择对化学选择性羰基化(2aa vs 2aa’)同样至关重要。在另一组底物1a的氘标记实验中(图5C,右),氘仅标记α位(60%),β位无标记,支持Pd-H物种对1a中乙烯基的β-选择性插入是不可逆的。在1a与甲醇反应的动力学曲线中(图5B),可观察到明显的诱导期,这可能归因于Pd(II)还原为Pd(0)生成Pd-H物种的过程。随后,伴随底物1a被消耗,目标产物2aa的产率逐渐升高,但其ee值始终保持在94%,并且反应历程中未检测到其他中间体。基于上述实验结果以及前人报道,作者提出了如图5D所示的催化循环。首先,由Pd(OAc)₂、L6和TsOH生成的Pd-H物种(I)对乙烯基进行β-选择性插入,形成烷基-Pd中间体II。随后,II与炔基发生5-exo-dig环化,生成轴手性烯基-Pd中间体III。接着CO插入将III转化为酰基-Pd中间体IV,后者被亲核试剂捕获,得到目标产物并再生Pd-H物种(I),完成循环。为进一步理解该反应的对映选择性,作者提出了决定手性步骤(中间体II)的空间模型(图5D,右)。较大的取代基RL占据开放空间位置,而较小的取代基(RS)被限制在受阻区域。因此,苯环两侧的空间位阻差异(RL vs RS)对反应的手性诱导起决定性作用。这一解释合理说明了2ka中由于RL与RS位阻差异极小,仅获得中等er值(84/16)。此外,从2ba、2ca、2aa、2da到2fa,对映选择性逐步提升(er从84.5/15.5增至99.5/0.5),也可归因于底物上取代基体积逐渐增大,这一点可通过相关的取代基参数加以分类(图5E)
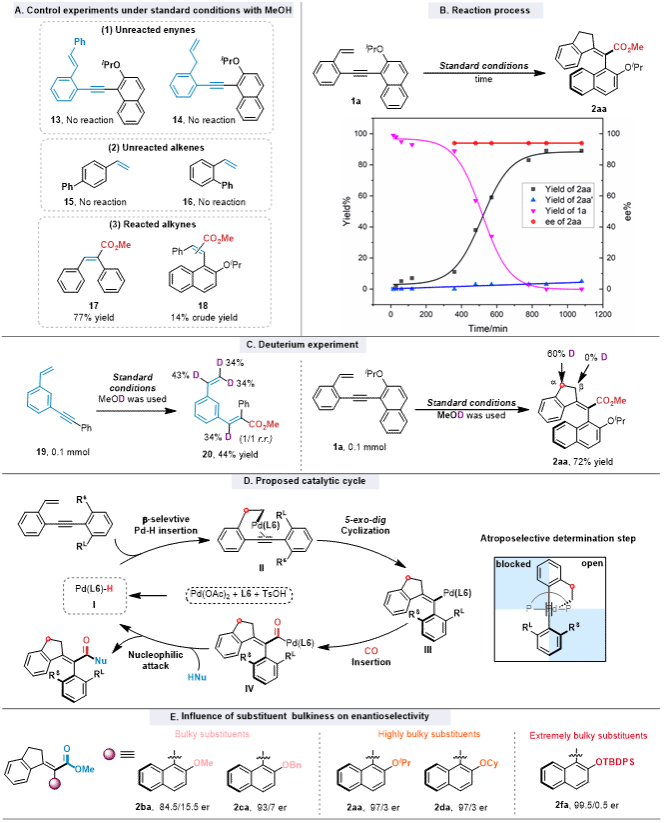
图5 机理研究
总之,该工作开发了一种高效的钯催化轴向选择性合成轴手性苯乙烯的方法,通过1,5-烯炔与CO及多种亲核试剂的非传统5-exo-dig环化/羰基化反应,构建构型超稳定的轴手性苯乙烯。该方法具有广泛的亲核试剂和官能团兼容性,以高对映选择性、中等到高的产率获得轴手性酯、羧酸和酰胺。值得注意的是,所得产物在高温下仍保持较好的构型稳定性。此外,产物可方便地转化为一系列轴手性衍生物,包括一种在不对称催化中表现出良好手性诱导能力的单膦配体。详细的机理研究也证明了作者在底物设计阶段的设想。本工作首次实现了由1,5-烯炔底物不对称合成构象稳定的轴手性苯乙烯,有望为手性分子设计带来新的突破。
上海交大学变革性分子前沿科学中心刘家旺副教授和高申助理研究员为本文共同通讯作者,上海交通大学变革性分子前沿科学中心2023级博士生杨熙为论文共同第一作者,上海交通大学为第一工作单位。该工作得到科技部重点研发计划、国家自然科学基金、中央高校基本业务费、交大2030计划以及上海市启明星计划支持。
导师介绍:
刘家旺, 上海交通大学变革性分子前沿科学中心长聘教轨副教授,博士生导师,曾入选上海市海外高层次人才计划(2021)和启明星计划(2021)。2011年本科毕业于郑州大学化学学院,2016年博士毕业于中国科学院上海有机化学研究所。2017-2020年在德国莱布尼茨催化研究所从事博士后研究。2021年入职上海交通大学。研究方向聚焦新型配体的设计合成及其在低碳资源小分子催化转化中的应用,包括不对称催化与聚合。迄今已在Science, JACS, Angew. Chem., Nat. Commun.等国际顶级期刊发表研究论文近30篇,作为负责人主持科技部重点研发计划课题、国家自然科学基金青年和面上项目、上海市以及企业委托项目,担任《Green Carbon》和《有机化学》期刊青年编委。课题组尚有2026年春季/秋季入学“申请-考核”制博士生名额,欢迎具有有机合成化学、高分子合成化学、金属有机化学等相关背景的同学加入我们团队。请有意者发送简历和研究小结至liujw2020@sjtu.edu.cn。同时,课题组长期招聘有机合成化学、金属有机化学以及高分子合成化学等相关领域的博士后,待遇从优,欢迎感兴趣的同学随时邮件联系,招聘信息详见:https://fsctm.sjtu.edu.cn/info/1027/1451.htm








