

碳水化合物是自然界中最丰富且结构最为多样的生物分子之一,广泛参与多种生命过程。在众多糖衍生物中,C-糖苷因其C–C键带来的优异化学和代谢稳定性,相较于天然的O-/N-糖苷,在药物设计中备受关注。特别是C-羟甲基糖苷,兼具C–C键的稳定性与羟基官能团的修饰潜力,有望突破传统C-糖苷在“活性与稳定性难以兼得”方面的瓶颈。以甘露C-糖苷为例,R-构型的羟甲基C-甘露糖苷表现出优异的抗流感病毒活性(HAI = 31 nM),其效力是相应O-糖苷(HAI = 62 nM)的两倍;而其S-构型异构体活性骤降(HAI = 6000 nM),两者活性相差近200倍,显示出羟甲基构型对药效具有决定性影响。尽管C-羟甲基糖苷在药物开发中具有巨大潜力,现有合成策略仍面临选择性不足、底物范围有限等问题,亟需开发更高效、通用且经济的合成方法,以推动该类结构在药物化学和糖生物学中的广泛应用。
近年来,Ni/Co催化的不对称还原性格氏加成反应已成为构建手性醇分子的高效手段之一。针对C-羟甲基糖苷合成中普遍面临的选择性控制难题,上海交通大学变革性分子前沿科学中心朱峰课题组受到该策略启发,融合光氧化还原催化与钴催化,发展了一种芳基碘化物与糖基醛之间的不对称还原加成反应,构建了高效构筑C-羟甲基糖苷的立体发散性合成平台(图1)。本研究的创新在于系统性地探索糖基醛作为手性烷基醛的反应性能,有效克服了糖分子中官能团密集和连续手性中心带来的立体选择性控制难题,成功实现了两种立体异构体的可控合成。该策略不仅为手性羟甲基C-糖苷这一重要骨架的快速、多样性构建提供了一种新颖且可持续的合成途径,也为基于糖结构的药物分子设计与开发提供了一个具有广阔应用前景的新工具。
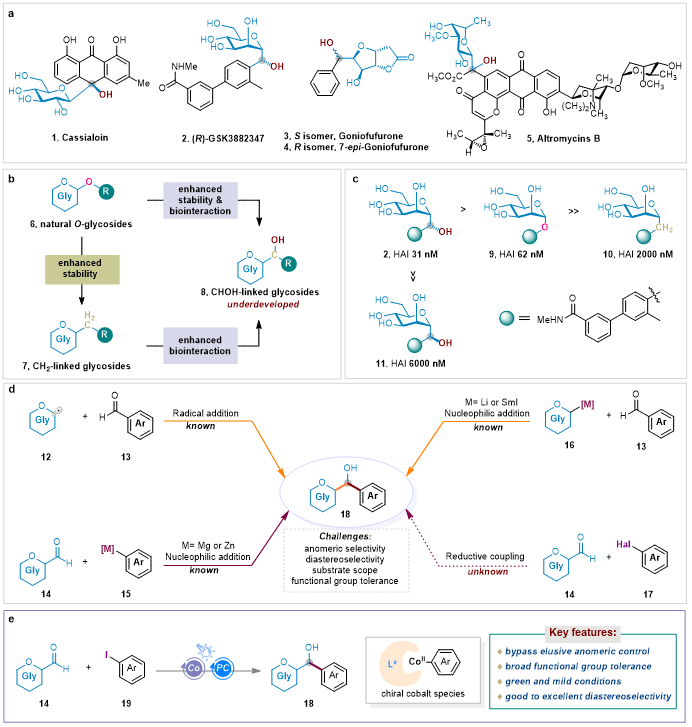
图1. 研究背景和设想
在优化反应条件下,作者对芳基碘代物的底物适用性进行了系统评估,所对应的C-羟甲基糖苷均以中等至良好的收率成功获得。研究结果表明,该反应体系对多种官能团具有良好兼容性,包括吸电子基团、给电子基团以及杂环结构,甚至在含药物分子结构单元的底物中亦表现出优异的适应性(图2a)。此外,该方法同样适用于不同类型的糖类底物,包括具有不同取代模式的五碳糖与六碳糖。值得一提的是,通过更换手性配体,可实现另一对映异构产物的选择性构建,进一步展现了该策略的立体多样性与广泛适用性(图2b)。
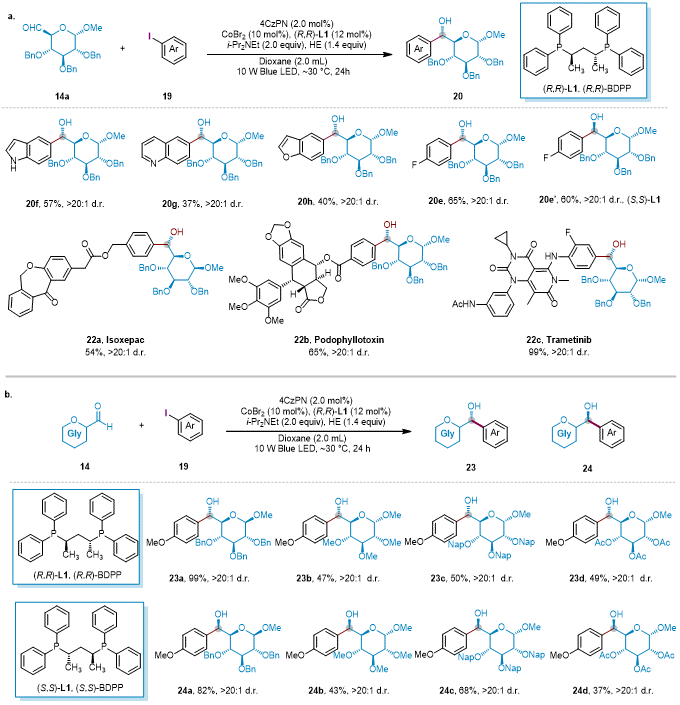
图2. 部分底物拓展
此外,作者进一步评估了该方法的合成应用潜力(图3)。通过放大反应、脱保护及多种衍生化操作,充分验证了该策略的实用性与可扩展性;同时,该方法可成功用于合成天然产物goniofufurone及其异构体7-epi-goniofufurone的前体分子。值得强调的是,该策略亦被应用于GSK公司抗菌药物候选分子GSK3882347的类似物合成,进一步彰显了其在药物分子构建中的广泛适用性与实用价值。
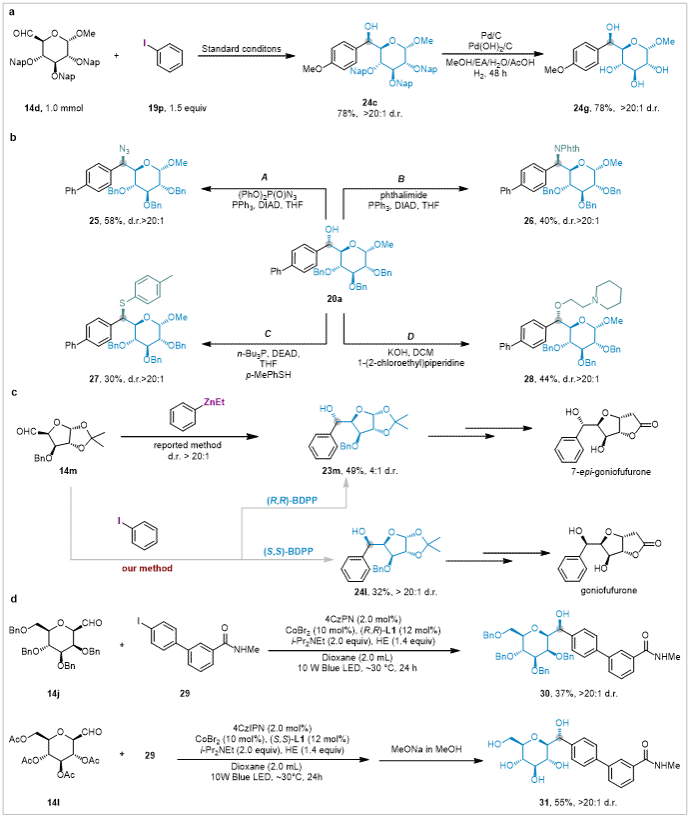
图3 合成转化
最后,作者提出了可能的反应机理,并结合DFT计算对其进行了深入探讨。研究表明,在主导的过渡态构型中,手性 Co(I)-芳基络合物与糖基醛之间存在更强的相互作用能,从而决定了反应的立体选择性(图4)。该结果不仅为理解钴催化剂在立体化学控制中的关键作用提供了重要的机理依据,也进一步凸显了该通用且稳健的催化体系在立体选择性糖基化反应中的应用潜力。
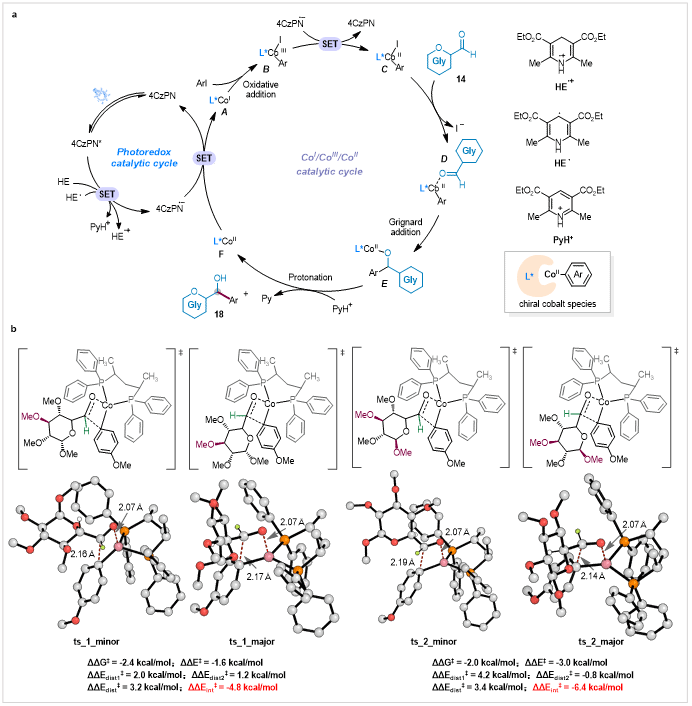
图4 机理研究
综上所述,朱峰团队开发了一种光诱导Co催化的不对称还原偶联新策略,实现了糖基醛与芳基碘化物的高效耦合,成功构建了C-羟甲基糖苷的立体发散性合成平台。该方法在温和条件下适用于多种五/六碳糖基底物,具有优异的产率、对映选择性和广泛的底物兼容性。其独特优势在于:(1)羟甲基的立体选择性构建完全不受芳基碘的影响,通过切换手性配体即可灵活获得目标产物的两种立体对映体;(2)结合DFT理论揭示了糖基醛对立体选择性的调控机制。该工作不仅为功能化C(sp³)-糖苷的合成提供了全新策略,也为糖基化药物的分子设计与开发构建了新型催化平台。相关成果以" Photoinduced Cobalt-Catalyzed Reductive Addition of Glycosyl C-Aldehydes: Stereoselective Synthesis of C-Hydroxymethine Glycosides"为题发表于《CCS Chemistry》。变革性分子前沿科学中心博士生赵诗音为论文的第一作者,朱峰副教授、杨波助理研究员,加泰罗尼亚化学研究所李英姿博士、南京中医药大学年永副教授及南京师范大学谢兰贵教授为共同通讯作者。上述研究工作得到了科技部重点研发项目青年科学家项目、国家自然科学基金及上海市科委等资助。
全文链接:https://www.chinesechemsoc.org/doi/epdf/10.31635/ccschem.025.202505656








