

手性β-芳基乙胺类化合物在药物化学和生物活性分子中占有重要地位,它们是许多天然产物和药物分子的核心结构,常常具有多样的药理活性(图 1a)。因此,如何高效且精确地合成这些手性分子,是有机合成领域长期关注的课题。尽管已有一些方法实现了手性β-芳基乙胺的合成,如刘国生课题组(图 1b)、Stephenson课题组(图 1c)和Nevado课题组(图 1d),但它们都依赖于过渡金属催化剂或需要难以合成的手性亚砜试剂,并且烯烃底物主要集中于活化烯烃。因此,同时实现高效、立体选择性和广泛适用性的手性β-芳基乙胺合成仍然是一项挑战。新试剂的创新有望避免过渡金属的使用以及扩大烯烃的底物范围,增强产物的多样性。
针对这一挑战,上海交通大学朱晨教授课题组设计并合成了一类全新的手性亚砜亚胺试剂,并成功应用于光诱导的烯烃不对称氨基杂芳基化反应,合成了一系列手性β-芳基乙胺类化合物(图 1e)。这些手性试剂不仅能够在温和的光照条件下生成氮中心自由基,而且实现了手性从硫原子向碳原子的精确转移。该反应的一个显著优势在于其广泛的底物适用性,不仅适用于(杂环)芳香烯烃,还可以高效地作用于脂肪烯烃。更为重要的是,该手性试剂可以很容易地进行克级制备。另外,该方法操作简单,无需使用过渡金属或光敏剂,极大地提高了其实用性和环境友好性。
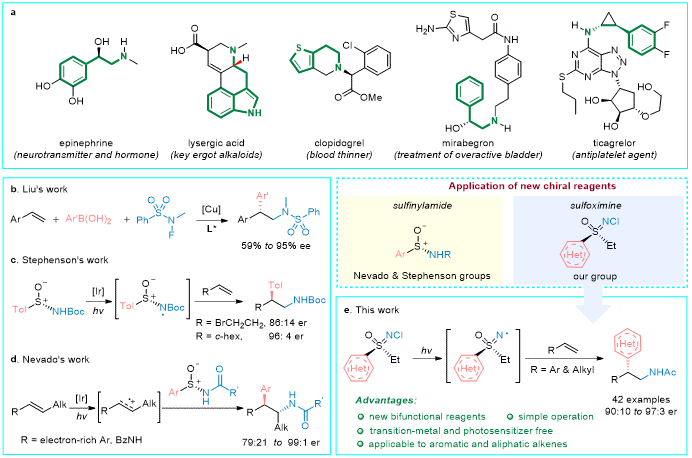
图1 含手性β-芳基乙胺骨架的天然产物和药物分子及其合成设计
在最优反应条件下,作者对不同类型的烯烃进行了详细的适用性研究。结果表明,无论是带有不同电子性质取代基的(杂环)芳香烯烃,还是含有敏感基团的脂肪烯烃,均能获得很好的反应产率和对映选择性。此外,多种迁移基团适用于该策略。通过对复杂分子结构的修饰,该方法展现出了在药物分子衍生物合成中巨大的应用潜力(图 2)。
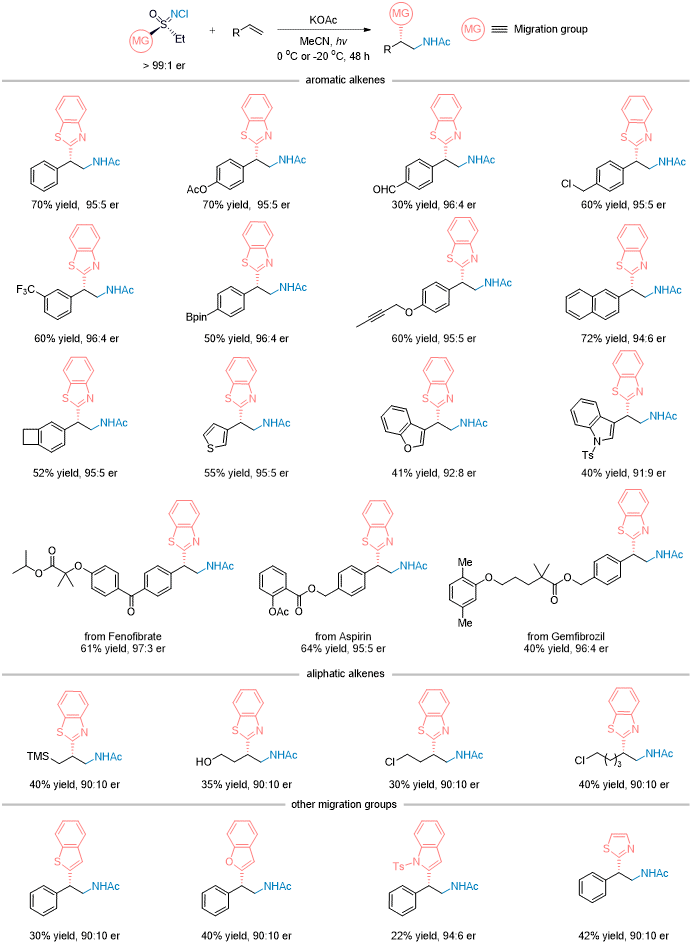
图2 底物拓展
在机理研究中,通过自由基捕获实验(图 3a)和自由基钟实验(图 3b),作者验证了自由基过程的存在,并通过光谱分析进一步支持了该反应的自由基途径(图 3c)。此外,作者分别使用氘代醋酸钾(图 3d)和甲酸钾(图 3e)代替醋酸钾,验证了产物中乙酰基的来源,并提出了可能的反应机理(图 3f)。

图3 机理探究
综上所述,朱晨教授课题组首次提出了使用手性亚砜亚胺试剂,通过光诱导实现烯烃的不对称氨基杂芳基化反应。这一反应为手性β-芳基乙胺的合成提供了一种高效且环境友好的新途径,并为未来进一步拓展自由基化学的应用奠定了基础。
该研究成果近期以“Photoinduced Asymmetric Alkene Aminohetarylation with Chiral Sulfoximine Reagents”为题发表在期刊《Angew. Chem. Int. Ed.》上(Angew. Chem. Int. Ed. 2024, 63, e202408177)。博士后曹柱为第一作者。上海交通大学变革性分子前沿科学中心朱晨教授为论文的通讯作者。本研究得到了国家自然科学基金(22171201和22371185)、中央高校基本科研业务费(22X010201631)、上海市学术/科技学科带头人计划(23XD1421900)和中国博士后科学基金(23Z020702964)的支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202408177








