


葫芦烷是一类广泛分布于葫芦科及其他植物中的次生代谢物,它们作为异源化学信息素,可以保护植物免受外部生物侵袭。如图1所示,从结构上看,葫芦烷类属于四环三萜类家族。这些高氧化态的葫芦烷类化合物通常具有多样的生物活性,包括抗肿瘤、抗炎和抗HIV病毒等。其中,cucurbalsaminones B (1) and C (2)是法国化学家Ferreira课题组于2019年从Momordica balsamina的甲醇提取物中分离得到的两个新型abeo-葫芦烷三萜类天然产物。与普通葫芦烷相比,cucurbalsaminones具有独特的5/6/3/6/5五环骨架,初步的生物活性研究表明它们具有较好的多药耐药(MDR)逆转活性。其在自然界中较低的含量(1的含量约为0.00024 wt %, 2 的含量约为0.00067 wt % ),独特的骨架结构,以及有趣的生物活性吸引了作者的合成兴趣。近日,上海交通大学吴晶晶副教授课题组成功实现了cucurbalsaminones B and C的仿生合成,相关成果发表在Angew. Chem. Int. Ed.上。
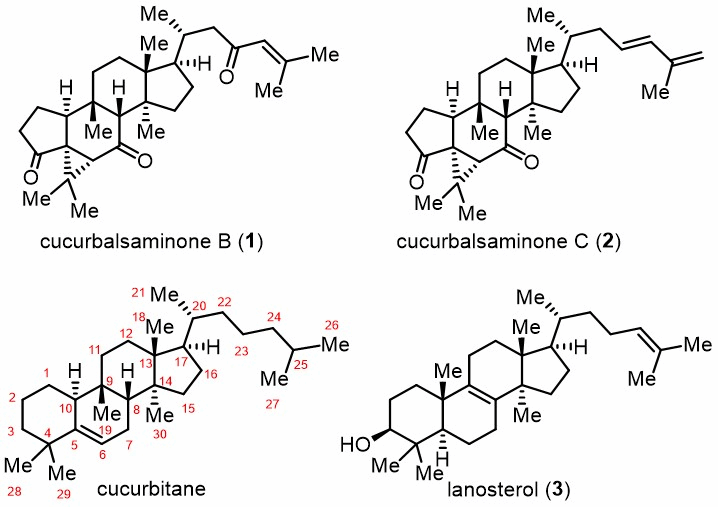
图1.
由于羊毛甾醇(3)是一类具有类似的四环三萜骨架且廉价易得的资源型化合物,作者拟将其作为起始材料,来进行合成。葫芦烷与羊毛甾烷的主要区别在于甲基在C9位而不是在C10位,生源合成上认为,葫芦烷是由羊毛甾烷重排而来,因此,作者也拟将这种仿生重排应用到合成中。此外,另一个挑战是如何将普通葫芦烷三萜的6/6并环的A/B环骨架,转化为天然产物所需的5/6/3三环骨架。分离问题提出的生源合成假说认为,酸催化的Michael加成型1,2-烷基迁移,得到烯醇负离子-碳正离子型 Zwitterion型中间体,再通过分子内烷基化形成环丙烷环。作者根据此生源合成假说进行尝试,均没有得到想要的目标产物。基于作者课题组在光化学领域的研究兴趣,作者设想了一种光化学oxa-di-π-methane(ODPM)的重排方法来构建天然产物的5/6/3三环体系。值得注意的是,在类似的甾体化合物中,已经有关于ODPM重排的报道(如图2a),但它们具有明显的局限性。该反应利用高压汞灯,这可能降低了官能团的耐受性,因此导致反应收率均低于30%。此外,根据Schaffner的结果,得到了α/β-两种环丙烷的混合物,这意味着这种ODPM重排可能具有较差的非对映选择性。作者认为,这些例子中较差的非对映选择性可能是其底物构象的原因。由于葫芦烷化合物在立体化学上与甾体非常不同,经过构象分析(如图2b),作者认为在葫芦烷中,获得β-环丙烷所经历的中间体12,其C4位甲基与C9位叔碳具有较大的1,3-二直立键相互作用,难以生成,因此在葫芦烷底物中可能具有更好的非对映选择性。因此环丙烷的高非对映选择性可归因于反应过渡态的空间位阻效应。与之前甾体体系中的研究相比,本文研究的葫芦烷体系,在产率和选择性方面取得了显著突破。
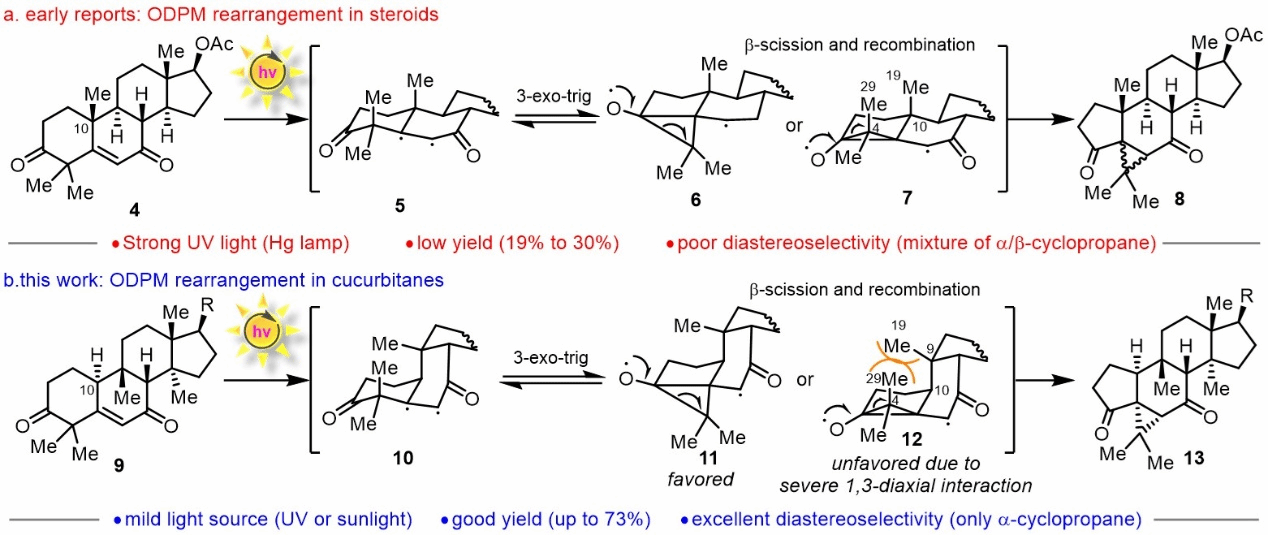
图2.
于是,作者从羊毛甾醇出发,来进行合成。首先C3位羟基乙酰基保护,然后侧链溴甲醚化保护,得到18。 随后依次经铬酰氯氧化、环氧化得到化合物17,然后经过仿生的Wagner-Meerwein重排构建C9位甲基,成功实现从羊毛甾烷到葫芦烷骨架的转化得到化合物22,后者经过选择性脱C3位乙酰基、PCC氧化,得到了A/B并环的6/6环葫芦烷三萜化合物16(如图5)。

图3.
之后作者尝试光化学oxa-di-π-methane(ODPM)重排构建天然产物的5/6/3三环体系。如表1所示,作者首先尝试在紫外光254nm条件下进行实验,可以以较好的收率得到单一的非对映异构体化合物23,之后作者发现在275、310和365nm波长下均可以以中等收率得到想要的目标产物,让人欣喜的是,该反应在390nm条件下也能很好进行。然而在455nm的可见光条件下,即使是使用了光催化剂Ir[(dFCF3ppy)2dttbpy]PF6,反应依然不能进行。考虑到太阳光中亦包含7%左右的紫外光,令人惊喜的是,作者将反应置于室外,在太阳光照射条件下也可以以较好的收率得到目标产物。基于以上实验结果,作者推测光化学oxa-di-π-methane(ODPM)重排更可能为该类天然产物的生源合成途径。
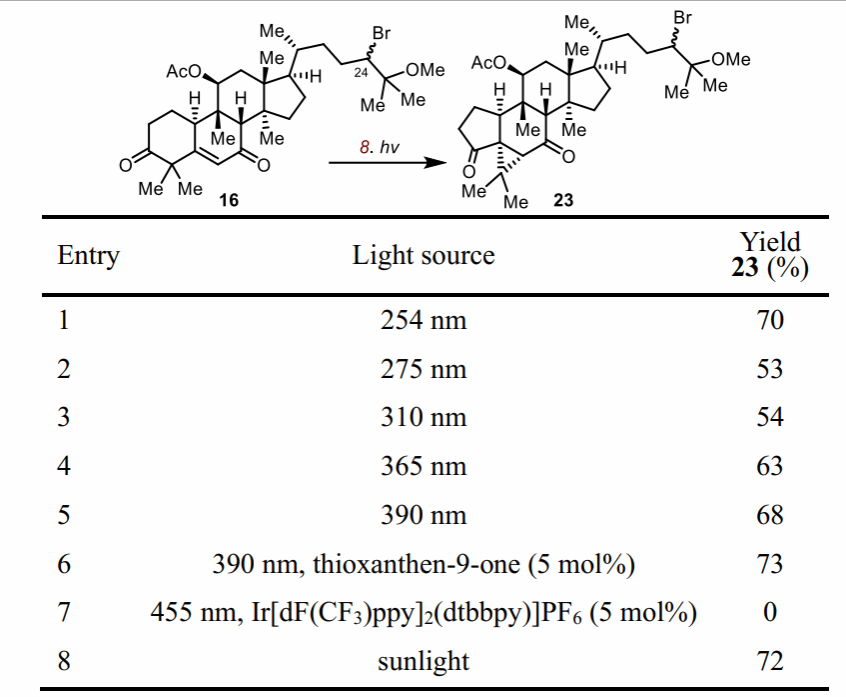
表1.
得到化合物23之后,作者尝试调整C11位的氧化态,首先脱掉C11位乙酰基,锌粉还原得到C24,25双键化合物25,由于C11位位阻大,作者经过一系列尝试,最终在MeLi条件下与CS2,MeI反应,能以较好的收率得到巴顿酯化合物15。
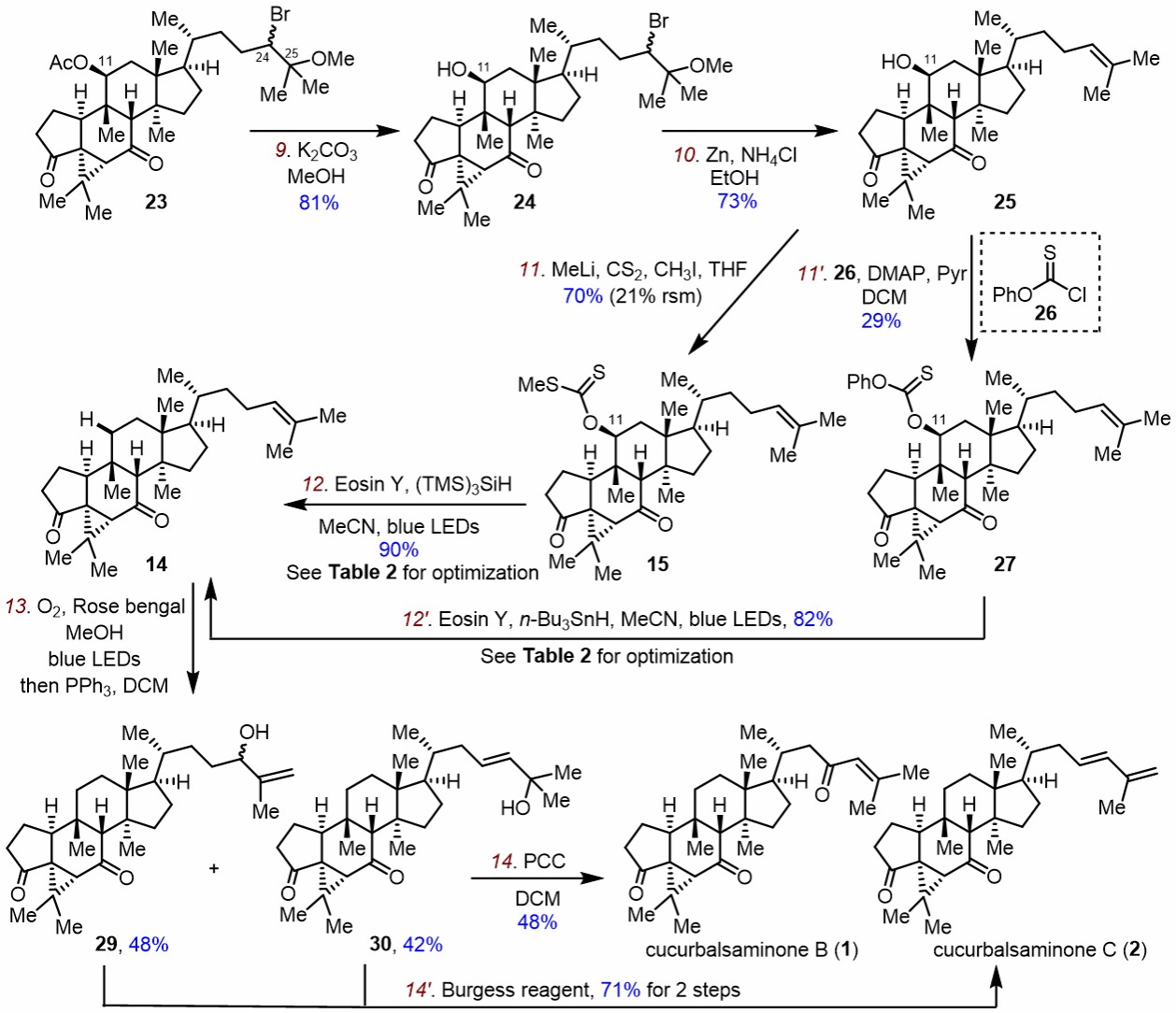
图4.
之后,作者尝试巴顿脱氧反应,在经典的巴顿脱氧条件下均得到消除产物(如图5所示)。基于在光化学领域的研究兴趣,作者发展了一种Eosin Y光催化的Barton-McCombie脱氧反应,成功实现了大位阻、高度拥挤的C11位羟基的脱除反应,有效避免了常规加热条件下的Chugaev消除副反应。作者通过量子产率测定实验,进一步证实了该反应经历了自由基链式历程。
成功实现C11位脱氧后,作者对支链进行改造。如图4所示,化合物14经过Schenck ene反应,还原,Burgess脱水得到了天然产物cucurbalsaminones C,化合物30通过[3,3]-sigmatropic Dauben-Michno 重排得到了天然产物cucurbalsaminones B。
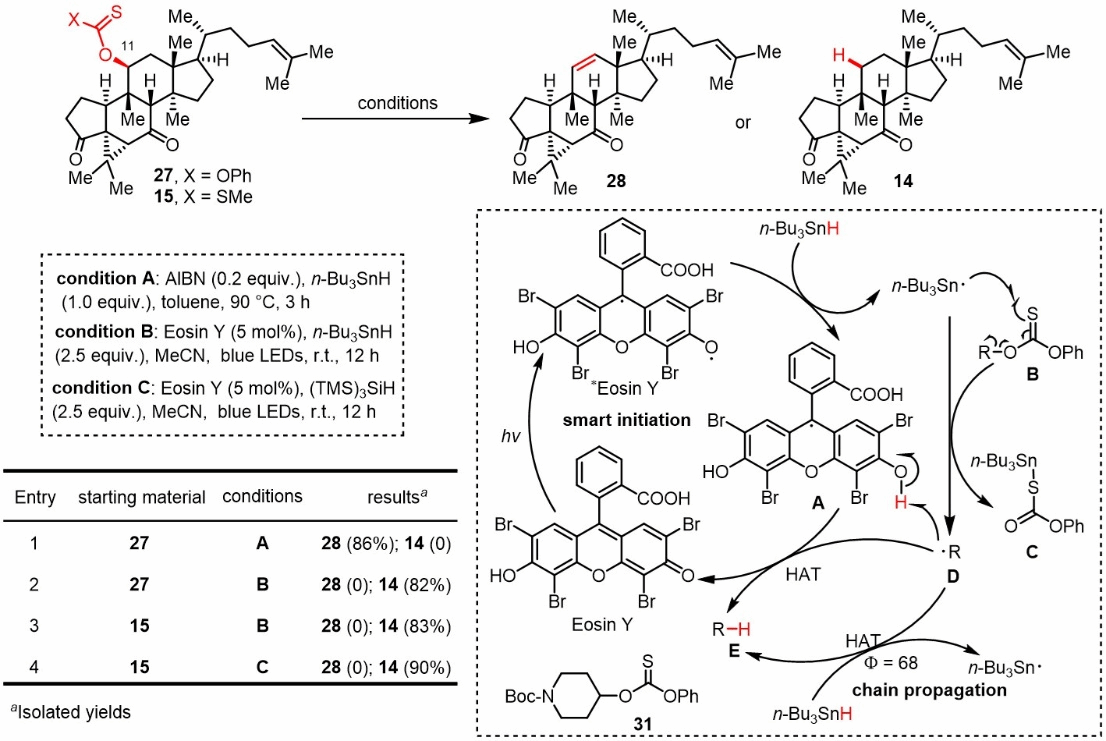
图5.
综上所述,吴晶晶课题组以廉价易得的资源型化合物羊毛甾醇为原料,以总步骤14步首次完成了天然产物cucurbalsaminones B和C的仿生合成。作者通过仿生的Wagner-Meerwein型lanostane-to- cucbitane重排,和新颖的光化学ODPM重排完成了天然产物骨架的构建。作者进一步证明光化学自由基重排过程更有可能为该类天然产物的生源合成途径。此外,作者还开发了一种Eosin Y介导的光化学Barton-McCombie的脱氧方法,成功地抑制大位阻的巴顿酯的Chugaev消除。
该研究成果近期以“Bioinspired synthesis of cucurbalsaminones B and C”为题,在《Angew. Chem. Int. Ed.》上线发表(DOI: 10.1002/anie.202417318)。上海交通大学博士研究生张孟晴为论文第一作者,上海交通大学吴晶晶副教授为论文的通讯作者。作者特别感谢英国布里斯托大学的Varinder K. Aggarwal 教授、上海有机所桂敬汉研究员和南洋理工大学Phillip. S. Grant助理教授在文章写作中所提供的帮助。感谢上海交通大学张兆国教授分享实验室。








