

由于脂肪胺在有机化合物中广泛存在,在合成化学中对于C(sp3)-N键的构建一直处于一个不可或缺的重要地位。目前已经发展了一系列经典的合成方法(图1a),比如Mitsunobu反应、烷基卤代烃及其类似物的亲核取代反应以及还原胺化反应。然而这些方法在反应条件、反应选择性和底物普适性上依然存在问题,这也激励着化学家去探索更加高效的、适用于复杂化合物的合成方法。考虑到脂肪酸在自然界中含量丰富、商业易得、毒性低而且化学稳定性好,以羧酸为原料构建C(sp3)-N键的方法得到了合成化学家关注。
然而,目前的进展主要集中于光化学领域(图1b)。在电化学脱羧胺化反应中,羧酸主要是经由阳极连续氧化生成碳正离子中间体与氰基或含氮杂环反应实现胺化(图1c)。由于碳正离子的高活性,需要杂原子或者不饱和键增加其稳定性,保证反应顺利进行。另外,羧酸的氧化电势较高,对官能团的兼容性也存在一定问题。最近,上海交通大学变革性分子前沿科学中心商明课题组报道了电化学镍催化脱羧还原交叉偶联构建C(sp3)-N键的新方法(图1d)。利用还原偶联的策略,绕过碳正离子中间体,在电化学脱羧胺化反应中开辟了一条新的路径。这一成果近期发表在Angew. Chem. Int. Ed上, 博士生蔡悦铭为论文的第一作者。
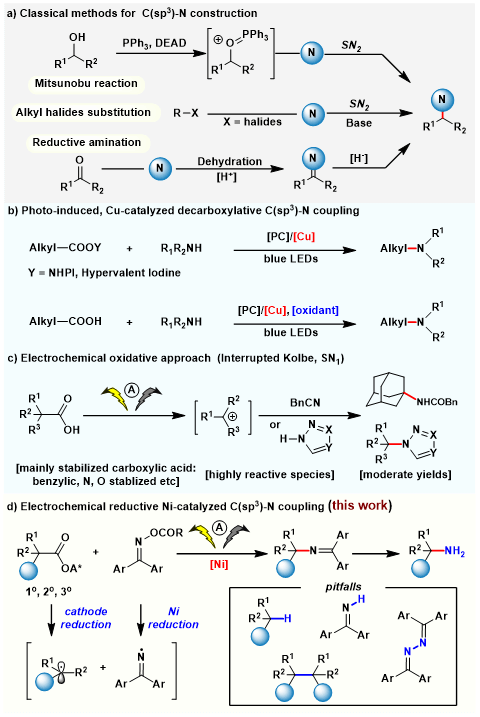
图片1
作者以脂肪酸活性酯衍生物和二苯甲酮肟酯为底物,NiCl2·glyme为催化剂,1,10-菲啰啉为配体,KPF6为电解质,锌片和泡沫镍分别为阳极和阴极,N,N-二甲基甲酰胺和异丙醚为混合溶剂,室温、氮气氛围下,3 mA反应5小时,以73%的收率得到亚胺化合物3。随后作者对底物进行了拓展。如图2所示,链状(3-5)和环状(6-11)亚胺化产物都可以中等至良好的收率得到。值得一提的是,一系列2-苯基丙酸(13-21)包括苄位羧酸(22,23)衍生物都可以顺利发生转化,以较高的收率得到产物。含有多种官能团的一级脂肪酸,比如酯基(25),苯氧基(26),羰基(27),氨基酸酯(28),以及杂环(29),在该体系下都可以较好的兼容。同时,作者也尝试了更有挑战性,位阻更大的三级羧酸,令人高兴的是,这些底物在电反应条件下也顺利得到了产物。为了证明该方法的实用性,作者尝试了对药物分子及天然产物(36-43)进行修饰,都能以中等至良好的收率得到亚胺化的产物。

图片2
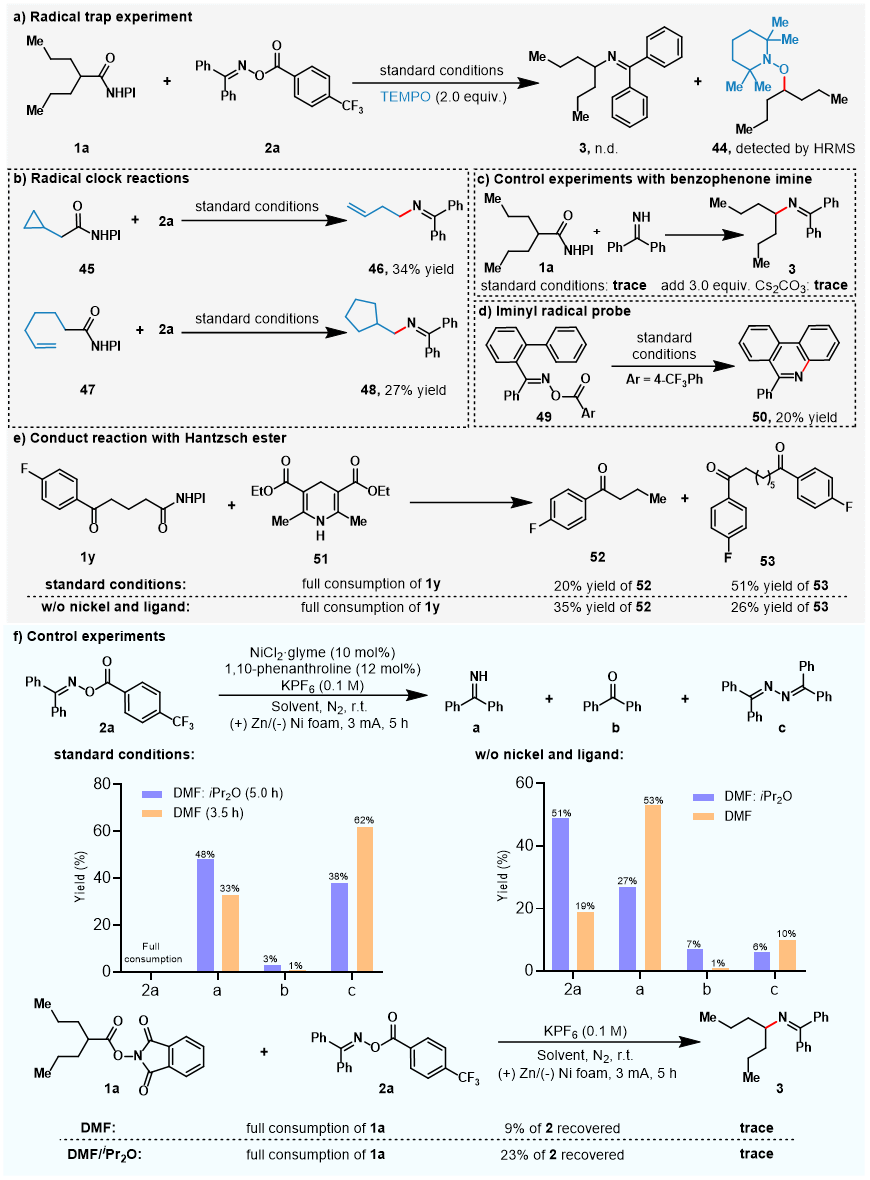
图 3
随后,作者对反应的机制进行了探究(图3)。作者通过自由基捕获实验(图3a)以及自由基钟实验(图3b)证明了羧酸活性酯在电反应条件下脱羧产生了碳自由基中间体。作者用二苯甲酮亚胺代替二苯甲酮肟酯(图3c),即使在加入3当量Cs2CO3作为碱的条件下,依然只有痕量的产物被监测到,排除了肟酯是以二苯甲酮亚胺负离子的形式参与到反应中。同时,作者运用分子内环化反应(图3d)验证了反应中亚胺自由基的生成。通过实施一系列控制实验以及循环伏安法实验,证明了羧酸活性酯主要是由电极直接还原生成自由基,而亚胺自由基的生成主要经由低价镍的参与。同时以异丙醚作为混合溶剂可以减缓亚胺自由基的生成,实现碳自由基和亚胺自由基生成速率的相对匹配,从而提升反应效率。基于机理探究实验以及前人的文献报道,作者对反应机理进行了推测。活性酯主要在阴极上直接被还原,得到烷基自由基A。肟酯被低价镍还原得到亚胺自由基B,接着亚胺自由基被Nin捕获得到中间体C。C与生成的烷基自由基A结合,得到高价镍物种D,然后发生还原消除,实现C(sp3)-N键的形成。
综上所述,作者报道了电化学促进的脱羧C(sp3)-N还原交叉偶联反应,该反应条件温和,具有较好的底物普适性,可以适用于一级,二级以及三级脂肪酸,同时可以兼容比较复杂的天然产物与药物分子。作者通过机理实验,阐明了反应的机制以及电极、镍催化剂和混合溶剂异丙醚在反应中起到的作用,为烷基胺类化合物的合成提供了新的解决方案。这一方法有望实现核苷酸类化合物的高效后期修饰,相关研究正在进行中。
原文链接:https://doi.org/10.1002/anie.202315222








