

近日,上海交通大学变革性分子前沿科学中心朱峰 副教授和美国科罗拉多大学博尔德分校化学系的Maciej A.Walczak教授合作,基于前期工作基础发展了新一代更加绿色、安全和高效的金属化丙氨酸试剂-丙氨酸硼试剂AlaB,成功实现了一系列非蛋白氨基酸、多肽的发散性后期修饰以及蛋白分子泛素的丙氨酸硼修饰。相关研究成果以“Synthesis of Non-Proteogenic Amino Acids, Peptides, and Proteins with AlaB Reagents”为题发表于杂志《Angew. Chem. Int. Ed.》上。
多肽和蛋白质作为一类重要生物活性分子,因其具有易合成、低毒性和靶点选择性等特点,而成为现代药物发现的重要靶点。 然而,天然肽通常表现出生物利用度低、化学和酶解稳定性差,这限制肽类生物治疗剂更广泛的应用。 为了应对这些挑战,非蛋白氨基酸 (Non-Proteogenic Amino Acids, NPAA) 作为一类非基因编码氨基酸,已成为增加结构和功能多样性和改善药代动力学特性的重要工具。目前,NPAA 的制备方法主要是 Strecker 反应、不对称氢化、共轭加成、生物转化、 光氧化还原交叉亲电偶联、C-H 活化 和相转移烷基化。尽管上述研究方法已取得了显著进步,但仍存在明显的底物局限性和难于精准控制α-位手性中心等挑战。为精准合成结构确定、成分均一的多肽和蛋白质,迫切需要发展高效的化学和立体选择性的后期衍生化方法。
2021年,朱峰副教授和Maciej A.Walczak教授合作将极性翻转策略引入到多肽修饰中,开发一类新颖的丙氨酸金属试剂-烷基笼状锡试剂AlaSn。该方法通过钯和铜催化的C-C、C-S、C-Se交叉偶联反应,成功实现了一系列高效的多肽、环肽和寡肽的发散性后期修饰以及精准控制化学和立体选择性(Chem Catal. 2021, 1, 870)。值得注意的是,AlaSn合成子应用到更为复杂的蛋白质修饰中依然充满挑战。
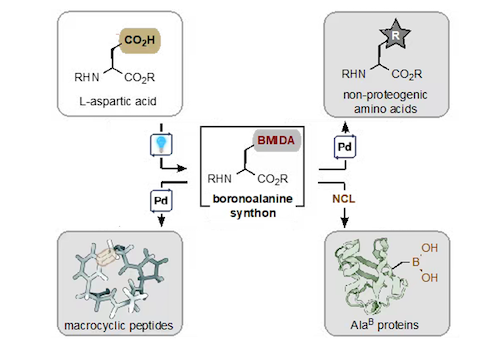
最近,双方进一步合作并发展了新一代丙氨酸金属试剂-丙氨酸硼试剂AlaB。令人意外的是,该功能化氨基酸合成子AlaB不仅适用于经典液相和固相多肽合成,而且能兼容一系列的酸碱操作,表现出令人印象深刻的化学稳定性。为此,作者进一步研究利用其合成或修饰氨基酸、多肽和蛋白质的可能性。首先,他们实现了从具有氧化还原活性的天冬氨酸酯顺利制备一系列丙氨酸硼衍生物AlaB。接下来,他们展示了 AlaB可以应用到寡肽和蛋白质的自动固相合成中。AlaB能兼容多肽合成中常见的各种化学转化操作,例如通过自然化学连接和自由基脱硫顺利实现丙氨酸硼修饰的泛素 (Phe4-AlaB) 的全合成。最后,通过AlaB试剂参与的Pd 催化C(sp3)-C(sp2) 交叉偶联和大环化反应,成功实现了一系列多肽的发散性后期修饰和环肽的高效制备。上述实验结果充分说明AlaB合成子是一类制备非天然氨基酸、修饰肽和蛋白质以及合成环状/钉合肽的实用试剂。
该工作增加了金属化氨基酸试剂的种类,丰富了多肽和蛋白质的结构修饰工具库,进一步证明极性翻转策略在多肽和蛋白质后期化学衍生化的巨大潜力。通过与DNA编码化学文库(DEL)和生物偶联技术等其他新兴多肽修饰技术的交叉融合,有望在新生物材料、治疗药物和探针的快速研发产生更深远的影响。
上海交通大学为第一完成单位,朱峰副教授为第一作者。
论文链接:https://doi.org/10.1002/anie.202207153








