

近日,上海交通大学变革性分子前沿科学中心的商明课题组开发了一类新型大位阻手性双噁唑啉配体,实现了首例氨基酸和多肽衍生的吡啶盐与非活化烯烃的不对称脱氨烷基化反应(图1c),相关工作发表在Journal of the American Chemical Society 上。
烷基胺广泛存在于生物活性分子、药物分子,有机材料分子以及一些高附加值有机化学品中。在此驱动下,化学家近几年来开始探索通过使用烷基胺化合物代替烷基卤代烃,通过sp3 C–N键的切断来构建sp3碳中心骨架。最近Watson课题组开发了以烷基胺的吡啶盐衍生物作为底物,在镍催化下构建了一系列的碳碳键和碳杂键。尽管已经取得了一些进展,但是sp3 C–N键的催化不对称官能团化反应还无法很好地实现。迄今为止,报导的方法都是从光学纯的手性胺出发,通过立体专一性反应构建sp3碳中心,并且底物局限于苄位,烯丙位,炔丙位(图1a),而利用消旋的底物通过立体收敛方式实现不对称脱氨官能化的反应还未有报道。主要原因是不对称脱氨sp3偶联反应具有以下挑战:首先,吡啶盐的脱氨活化多经历单电子转移机理,其立体选择性较难控制,并且消旋底物的不对称脱氨偶联反应未有报道,可参考文献较少;其次,反应中会生成当量的三苯基吡啶副产物,可能会竞争手性配体与金属的配位,从而降低产物的对映选择性;第三,不同取代烯烃及内烯烃潜在的区域选择性问题。
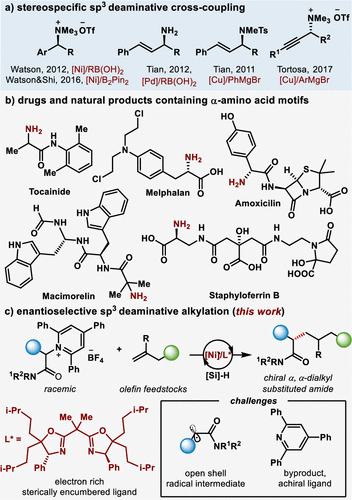
图1. 不对称脱氨烷基化反应介绍
由于α-氨基酸骨架在天然产物、药物及生物活性分子中普遍存在(图1b),作者选择使用α-氨基酸的吡啶盐衍生物以及廉价易得的非活化烯烃作为sp3亲核试剂前体来尝试不对称脱氨偶联反应,构建sp3-sp3骨架。经过一系列的条件筛选(图2),以96:4 er 和86%的产率得到了脱氨烷基化产物。值得一提的是,在配体筛选过程中,作者设计合成了一种新的大位阻双噁唑啉配体,提升了低温条件下反应的活性和对映选择性,这也是此反应得以实现的一个关键。
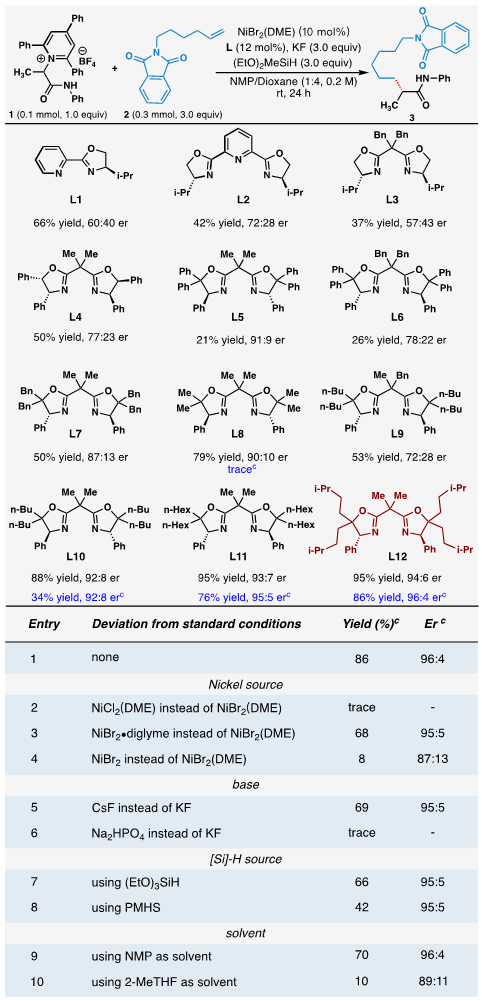
图2. 反应配体筛选和条件优化
在获得最优条件之后,作者对该反应的普适性进行了考察。首先考察了不同的非活化烯烃,如图3所示,该反应具有良好的化学选择性,例如含有卤素(4, 5)、酯基(6)、醛基(7)和醚键(8)的烯烃在反应体系中都可以很好地兼容。药物分子中常见的杂环骨架(14-18)以及非天然氨基酸(19)片段的底物也能以较好的收率和立体选择性得到产物。当底物中含有芳基硼酸(21)和芳基卤代烃(22)片段时也不会影响目标碳碳键的形成,为产物的进一步转化提供了很大空间。同时,该反应体系也适用于1,1-二取代烯烃(23-25)。更重要的是,环戊烯(26)和环己烯(27)等环状烯烃也能成功转化,实现了两个二级碳中心的sp3 C-C键的构建。
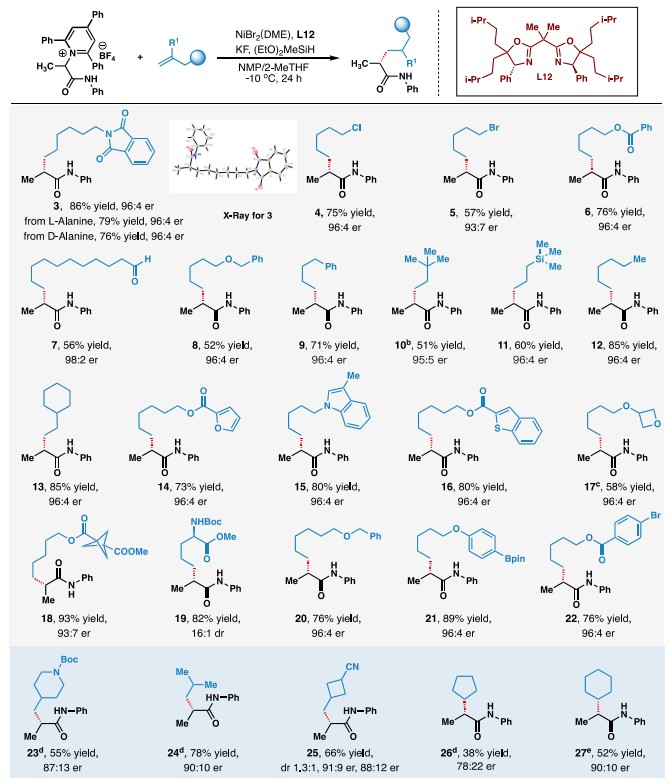
图3. 非活化烯烃底物范围
随后,作者考察了氨基酸吡啶盐的适用范围。如图4所示,2-氨基丁酸(28)和2-氨基己酸(29)能够以较高的产率和对映选择性得到产物。缬氨酸(30)、苯丙氨酸(31)、蛋氨酸(32)、赖氨酸(33)和谷氨酸(34)等天然氨基酸都能很好地适用,以及含有氟或溴的氨基酸(35, 36)和非天然氨基酸(37, 38)也能成功转化。不同单取代酰胺(39-45)以及二取代酰胺(46)在反应体系中都能够很好兼容。然而,当作者以氨基酸甲酯(47)和氨基酸叔丁酯(48)衍生物为底物时,对映选择性显著降低。表明酰胺结构对于该反应的对映选择性控制起重要作用。值得强调的是,该反应同样适用于多肽底物(49-53),为多肽修饰提供了一个重要手段。
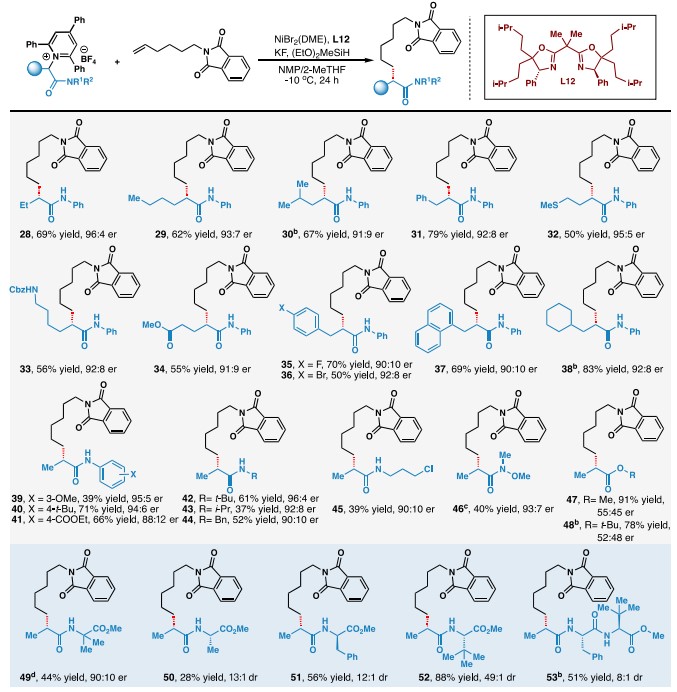
图4. 氨基酸和多肽底物范围
为了更好地探索反应的应用性,作者将此反应运用到了药物及天然产物的后修饰。如图5所示,香豆素(54)和樟脑磺内酰胺(55)等天然产物,消炎药(56, 59, 62, 67),抗菌药(66)及抗精神病药物(63)等都能高效地转化,说明此反应在新药研发领域具有较大潜力。
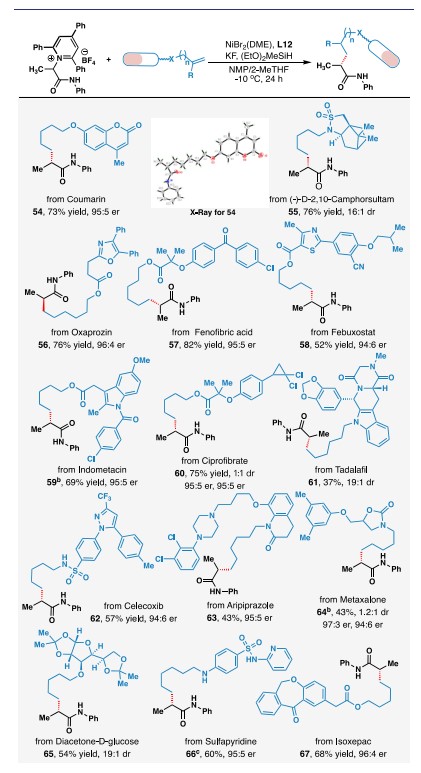
图5. 复杂药物分子的后期修饰
最后,作者还对难以控制区域选择性内烯的反应性进行了考察(图6a,68-71),通过镍氢迁移策略,实现了远程非活化C-H键的不对称官能团化。有趣的是,当使用等长碳链的混合烯烃(图6a, 72)作为原料时,能够选择性地得到同一产物。此外,将反应进一步放大,其产率及对映选择性未受影响(图6b)。在此基础上,作者也对产物做了一系列转化,得到了多种衍生物(图6c),进一步揭示了反应的实用性。
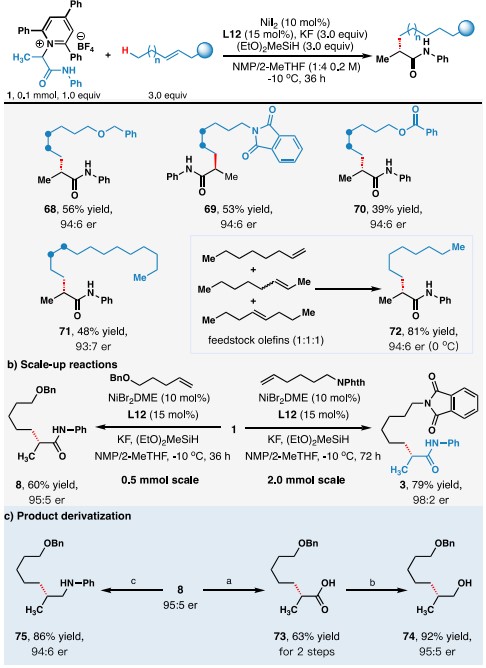
图6. 内烯烃反应和产物转化
商明课题组报道了首例镍催化的不对称脱氨烷基化反应,发展了一类新的大位阻双噁唑啉配体,提高了反应的效率,区域选择性和对映选择性。该方法以廉价易得的氨基酸和多肽以及非活化端烯或者内烯作为原料,为合成手性的α, α-二取代酰胺提供了一条快捷,高效的途径。此外天然产物和复杂药物分子的后修饰展示了该反应较好的应用前景。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.1c12350








