

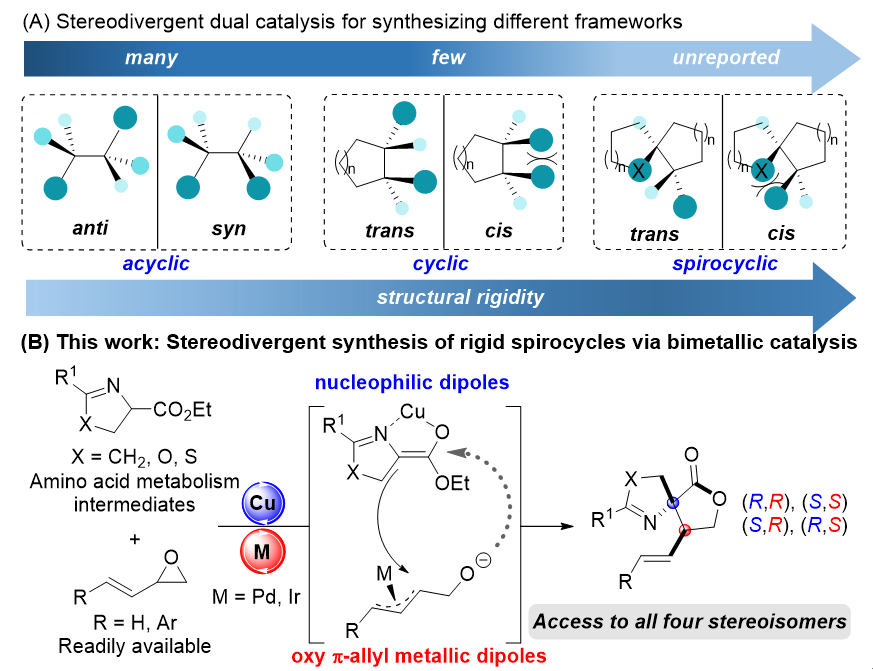
图1. 手性螺环骨架的立体发散性合成
手性螺环骨架分子由于其独特的三维空间结构以及较强的结构刚性,使得其在药物设计与手性配体开发中受到广泛关注。然而,由于其较强的环张力和较大的立体位阻,因此不对称催化合成螺环化合物是一个具有挑战性的研究课题。利用简单易得的化学原料来立体发散性地合成手性螺环分子则更加具有挑战性,且目前螺环骨架的立体发散性合成尚无报道 (图1A)。
氧𝜋-烯丙基钯偶极子与亲电偶极子的不对称环化反应是构建光学纯氧杂环状化合物的一种有效方法,不同类型的亲电偶极子如α,β-不饱和化合物、醛、亚胺等已被成功应用于该类反应中。尽管这种反应方式已经取得了长足的发展,但是对于亲核偶极子参与的环化反应面临极大的挑战。原因在于钯催化的烯丙基取代反应倾向于形成直链的烯丙基产物,使得氧𝜋-烯丙基钯偶极子与亲核偶极子的环化反应不易发生。而铱催化的烯丙基取代反应倾向于形成支链的烯丙基产物,这使得氧𝜋-烯丙基铱偶极子与亲核偶极子的环化反应的发生成为可能,但目前氧𝜋-烯丙基Ir偶极子与亲核偶极子的环化反应还未被有效开发 (图1B)。
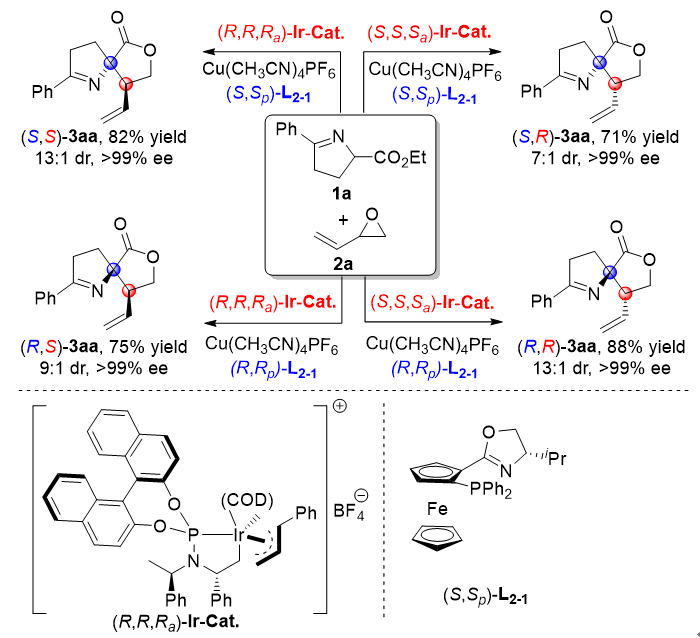
图2. 螺环化合物的立体发散性合成
上海交通大学张万斌课题组长期致力于双金属协同催化体系的开发及其立体发散性合成研究。在2016年, 该课题组报道了第一例基于双手性金属协同催化策略的立体发散性合成,成功开发了Ir/Zn 双手性金属协同催化体系,并实现了α-羟基酮的立体发散地烯丙基化 (J. Am. Chem. Soc. 2016, 138, 11093-11096),随后又陆续开发了Ir/Cu与Pd/Cu双手性金属协同催化体系,并成功应用于立体发散性合成 (J. Am. Chem. Soc. 2018, 140, 2080-2084; J. Am. Chem. Soc. 2020, 142, 8097-8103; CCS Chem. 2021, 3, 1933-1944; J. Am. Chem. Soc. 2021, 143, 12622-12632)。近日,张万斌课题组利用双手性金属协同催化的策略,首次实现了手性螺环化合物的立体发散性合成,并成功解决了氧𝜋-烯丙基铱/钯偶极子与亲核偶极子不对称环化反应中面临的区域和立体选择性难控制的问题 。
通过对金属盐及其手性配体的系统筛选,在以手性金属铱催化剂与手性Cu-Ferrophox催化剂组成的双手性金属催化剂下,2-乙烯基环氧乙烷与亲核偶极子酮亚胺酯的不对称[3+2]环化反应可以顺利地发生,以良好的收率,高的非对映与对映选择性得到螺环产物。仅仅通过改变手性金属铱催化剂和手性金属铜催化剂的构型组合,就可以很顺利地获得该螺环产物的所有立体异构体 (图2)。
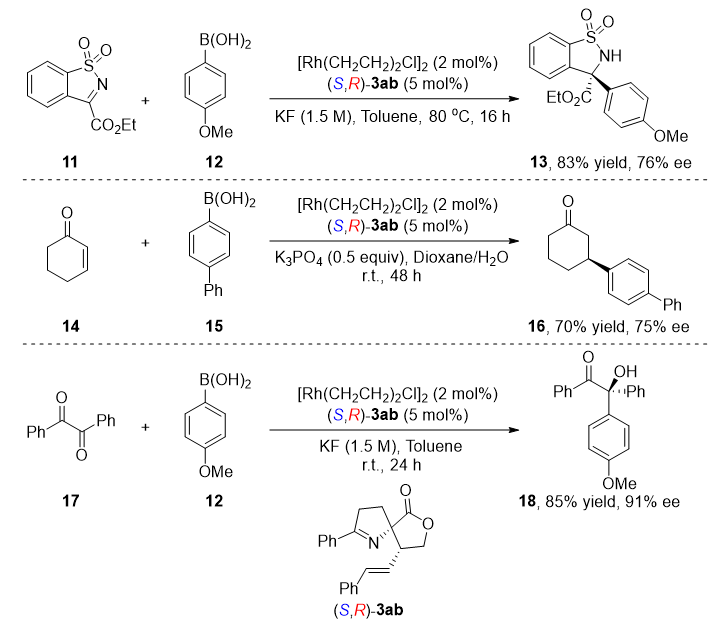
图3. 螺环化合物(S,R)-3ab作为氮-烯配体应用于铑催化的不对称芳基化
进一步的研究发现:该类手性螺环产物可以作为一类新型的手性氮-烯配体直接应用于金属铑催化的不对称加成反应中,并且产物可以获得优秀的对映选择性 (图3)。
总结:上海交通大学张万斌课题组利用双手性金属协同催化策略分别实现了2-乙烯基环氧乙烷和2-芳基乙烯基环氧乙烷与亲核偶极子的不对称[3+2]环化反应,首次实现了螺环骨架的立体发散性合成。同时该手性螺环产物可以作为一类新型的手性氮-烯配体,直接应用于铑催化的不对称加成反应中,表明该手性螺环产物具有极大的应用价值。机理研究揭示了双金属催化的协同过程。该反应也为新型手性环状化合物的合成提供了新思路。这一研究成果发表在Angew. Chem. Int. Ed.上。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202111842








